carbón dulce a los niños que se han portado mal. Si algún año no has
sido bueno y te ha tocado recibir este curioso producto, quizá te hayas
preguntado cómo se hace. O tal vez ni siquiera te lo hayas planteado
porque has supuesto que se trata simplemente de un gran trozo de azúcar.
Obviamente el carbón dulce contiene azúcar, pero es mucho más que eso,
ya que su elaboración, a pesar de ser relativamente sencilla, encierra
una serie de complejos procesos físico-químicos. En definitiva, el
carbón dulce no es lo que parece…
 |
| Si no fuiste bueno el pasado año, ya sabes lo que toca… (Fuente) |
El origen de la tradición
ir entrando en materia, veamos brevemente cuál es la historia de este
producto. Existen varias versiones acerca del origen de esta tradición
que, como sabrás, consiste en regalar carbón a los niños que se han
portado mal, a saber:
- Una de las versiones se basa en la figura de Carbonilla,
un paje de los Reyes Magos que, según la tradición, se encarga de
vigilar a lo largo del año a los niños y en la noche del 5 de enero les
deja carbón a aquellos que no se han portado bien.
- Otra versión se basa en la tradición que existía antes del siglo
XIX, cuando los Reyes Magos, en lugar de regalar juguetes a los niños,
se encargaban de regalar diferentes objetos de utilidad: Melchor repartía ropa o zapatos; Gaspar regalaba golosinas, requesón, miel o frutos secos y Baltasar repartía carbón o leña para castigar a los niños que se habían portado mal.
 |
| Mosaico de San Apolinar Nuovo (Rávena, Italia). (Fuente) |
Curiosamente, existen otras tradiciones
similares en distintas zonas geográficas que también se basan en el
carbón, Por ejemplo, en Italia existe la leyenda de la bruja Befana, que deja carbón a los niños que se han portado mal, mientras que en la zona de Lesaka (Navarra) existía la tradición del Olentzero,
un carbonero que vivía en el monte y al que no le gustaban nada los
niños (en el siglo XX este personaje incorporó ciertos elementos de Papá
Noel y los Reyes Magos, y la tradición se extendió por Navarra y el
País Vasco). Pero no nos dispersemos más y vayamos al grano.
La receta
No te pierdas el siguiente vídeo, en el que puedes ver el curioso proceso de elaboración del carbón dulce:
glacé real, para lo cual se mezcla una gran cantidad de azúcar glas con
varias claras de huevo y un poco de zumo de limón mientras se remueve
continuamente. También es necesario añadir colorante para dar color
negro al producto.
la mezcla aumenta de volumen se deja de remover y se vierte en un
recipiente de un tamaño adecuado para que pueda expandirse sin
problemas.
La ciencia que encierra esta receta
la receta ya no parece tan sencilla, ni mucho menos, ya que en el
conjunto de etapas que acabamos de ver tienen lugar numerosos procesos
físico-químicos, algunos de ellos muy complejos. Veamos.
sabrás, cuando se baten unas claras de huevo durante cierto tiempo,
éstas aumentan de volumen formando una espuma de color blanco, es decir,
alcanzan lo que se conoce como «el punto de nieve». Si lees asiduamente este blog,
sabrás que esto sucede porque al batir estamos incorporando burbujas de
aire en el medio, que son retenidas gracias a las propiedades de las proteínas globulares que contiene la clara de huevo.
 |
|
Las proteínas globulares son compuestos tensioactivos, con una parte hidrófila (con afinidad por el agua) y otra parte hidrófoba (que «rechaza» el agua).
|
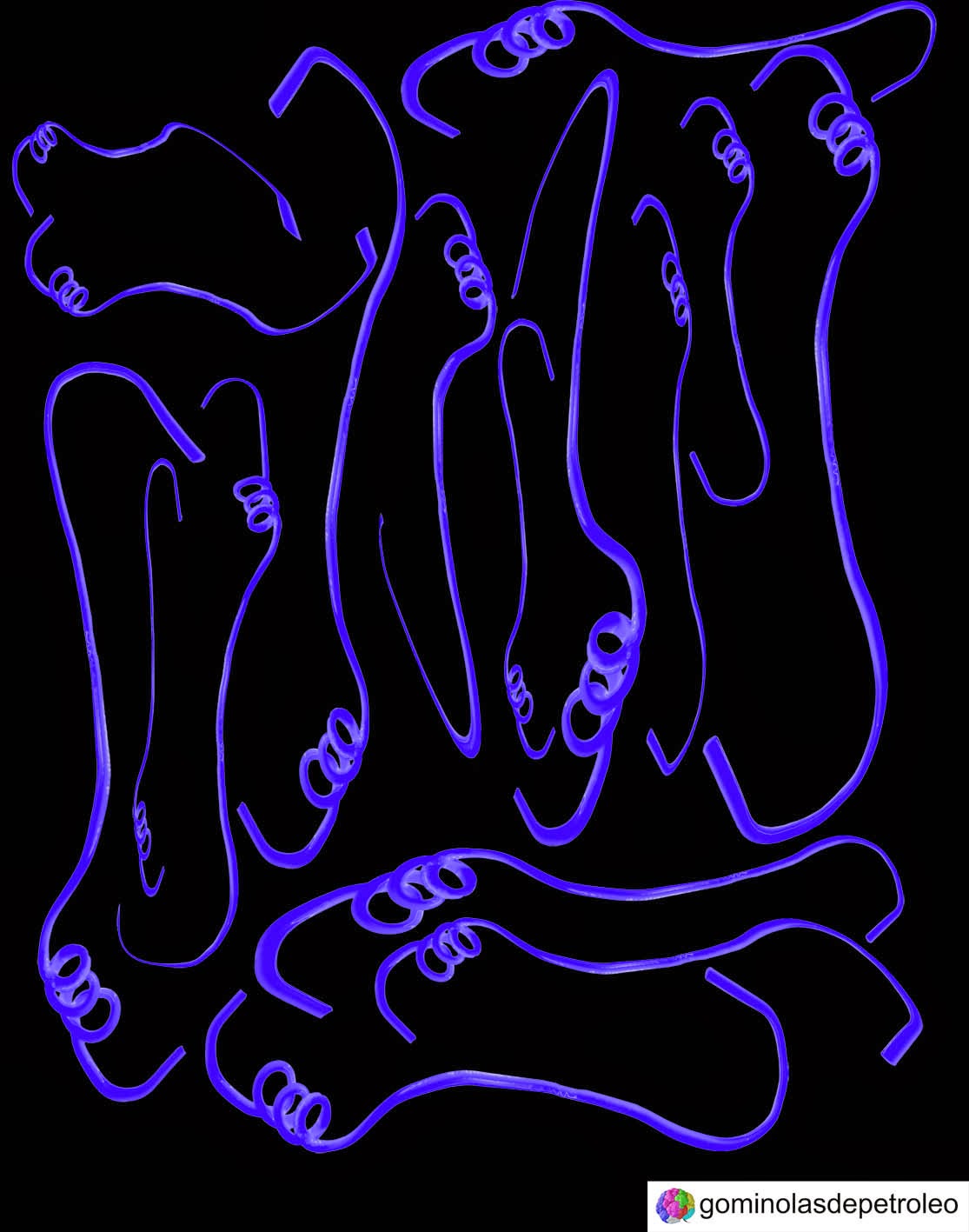 |
| Al batir, además de incorporar aire al medio, provocamos un desdoblamiento de las proteínas globulares, de modo que sus partes hidrófilas e hidrófobas quedan «expuestas». Así la parte hidrófila se sitúa junto al agua y la parte hidrófoba se aleja de ella. |
que no es otra cosa que la zona comprendida entre las dos fases que
constituyen el medio: el agua que compone la clara de huevo (fase continua) y las burbujas de aire que hemos incorporado al batir (fase dispersa).
De este modo, las proteínas globulares rodean las burbujas de aire,
haciendo posible su dispersión en el agua de la clara. En este fenómeno
tienen especial importancia dos de las proteínas que componen la clara:
la ovomucina y la ovotransferrina, debido a que se desdoblan fácilmente y se adsorben rápidamente a la interfase.
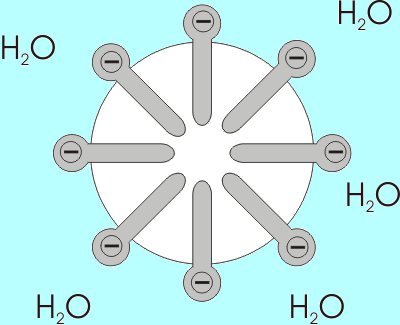 |
| Interacción entre las proteínas, el aire y el agua. (Fuente) |
ocurre cuando queremos hacer una glasa real, es decir, cuando añadimos
azúcar glas a las claras de huevo y batimos? En primer lugar, la mayor
parte del azúcar se disuelve en el agua que compone las claras (están formadas por aproximadamente un 88% de agua). Esto hace que aumente la viscosidad del medio, lo que dificulta la incorporación de aire, así como el desdoblamiento de las proteínas, la interacción entre ellas y su adsorción a la interfase.
Además, es probable que la ovoalbúmina (y seguramente el resto de las
proteínas globulares que componen la clara de huevo) forme puentes de hidrógeno con las moléculas de sacarosa, aumentando así la afinidad de estas proteínas por el agua y reduciendo su actividad superficial, por lo que en lugar de adsorberse a la interfase, permanecen en la fase continua. En definitiva, la adición de azúcar a la clara de huevo, retrasa la formación de espuma y reduce su fuerza
(es decir, disminuye la capacidad de la espuma para retener aire). Por
eso, en comparación con lo que ocurre en una clara a punto de nieve, la
glasa real no aumenta mucho de volumen cuando batimos (las burbujas que
se incorporan son pocas y de pequeño tamaño).
que hemos añadido? El limón contiene ácidos como el cítrico y el
ascórbico, así que se añade principalmente para provocar un descenso del
pH de la clara de huevo (su valor está en torno a 7,7 aunque puede
aumentar de forma significativa durante el almacenamimento del huevo
debido a la pérdida de dióxido de carbono a través de los poros de la
cáscara). Así se favorecerá la formación de un gel cuando se caliente la
mezcla (es probable que intervenga además en otros fenómenos que
veremos más adelante).
otra parte, tenemos una mezcla de azúcar y agua que calentamos hasta
130 ºC. ¿Por qué hasta esa temperatura y no hasta otra? Además, ¿no es
cierto que el agua hierve a 100ºC? ¿Cómo es posible entonces calentar
hasta 130ºC? La cuestión es que cuando añadimos azúcar al agua, el
número de moléculas disueltas es mayor, lo que hacer que aumente el
punto de ebullición. Esto significa que la temperatura puede indicarnos cuál es la concentración de la disolución. Así,
si representamos la relación entre el punto de ebullición y la
concentración de azúcar de la disolución, obtendremos una gráfica como
la siguiente:
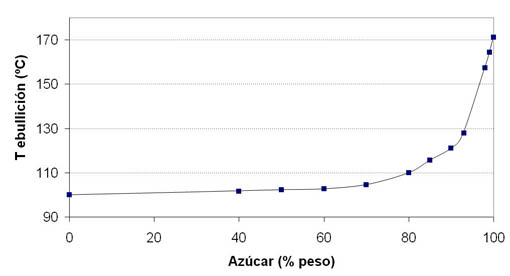 |
| En esta gráfica puedes ver la relación entre el punto de ebullición (ºC) y la concentración de azúcar (% en peso) al nivel del mar (McGee, 2004). |
producto que obtendremos cuando el almíbar se enfríe. Por ejemplo, si
contiene poca cantidad de azúcar obtendremos un almíbar suave como el
que se emplea para elaborar frutas en almíbar, mientras que si la
cantidad de azúcar es elevada, obtendremos un caramelo duro. ¿Cuál será
la concentración de azúcar necesaria para elaborar carbón dulce? Como
recordarás, el almíbar debe alcanzar unos 130ºC, lo que indica, según la gráfica anterior, que la concentración de azúcar es aproximadamente del 95%; cantidad con la que podremos obtener un caramelo duro cuando la mezcla se enfríe.
de la clara de huevo, es decir, se produce un desdoblamiento de su
estructura, exponiendo así parte de los aminoácidos que estaban
«encerrados» en el interior de las moléculas. Esto favorece las
interacciones intermoleculares, tanto entre los aminoácidos, como entre
los grupos sulfhidrilo que componen las proteínas. Así se forman
agregados que dan lugar a una estructura tridimensional elástica (gracias, en
parte, a la presencia de azúcares) que retiene las burbujas de aire que
introducimos al remover, así como parte del vapor de agua que se produce
por el calentamiento.
 |
| Las proteínas desnaturalizadas interaccionan entre sí para formar una red tridimensional. |
es probable que los ácidos del limón provoquen la hidrólisis parcial de
la sacarosa en los dos monosacáridos que la conforman: glucosa y
fructosa. A diferencia de la sacarosa, estos son azúcares reductores, de
modo que ahora tendríamos presentes en el medio todos los ingredientes
que hacen posible las reacciones de Maillard: aminoácidos,
azúcares reductores y calor. Dichas reacciones influirían, no sólo en el
sabor y el color del producto, sino también sobre su estructura. Por otra parte, se producen además reacciones de caramelización.
por proteínas que retienen agua y azúcares en su interior. Otro
importante fenómeno que tiene lugar es la cristalización de dichos
azúcares (o mejor dicho, su solidificación, presumiblemente en
estado amorfo), que otorgan a la estructura rigidez y dureza. La
hipotética presencia de glucosa y fructosa evitaría que el producto
adquiriese una estructura granulada.
la explicación es demasiado vaga, pero como ves, se trata de un tema
muy complejo y sobre el que no existe mucha información. Espero que al
menos te hayas dado cuenta de que a veces lo que parece sencillo no lo
es tanto.






es dulce