
Proteínas de la leche
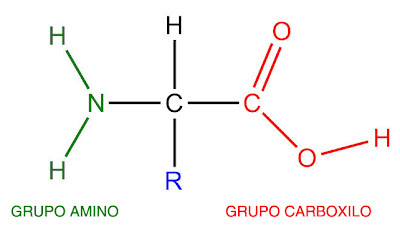
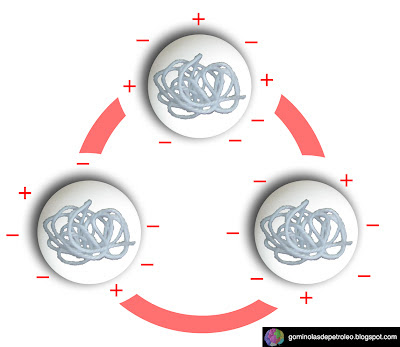
En la leche, las proteínas más importantes se llaman caseínas. Como ya vimos, estas caseínas se encuentran formando una dispersión coloidal, lo que significa que se encuentran en equilibrio en el seno del fluido. ¿A qué se debe este equilibrio? Lo entenderás mejor con esta imagen:
En la receta se indica que para hacer esta bebida primero hay que añadir hielo a la leche y luego ya se puede adicionar el zumo. La leche no se corta porque el punto isoeléctrico de las proteínas depende de la temperatura: por encima de 17º C la leche se corta a un pH de entre 5,2 y 4,7, mientras que si la temperatura es de 0º C se corta a pH=4,3. Es decir, en lugar de alcanzarse el punto isoeléctrico a pH 4,7, se alcanza a pH 4,3. Este fenómeno está relacionado con la estructura y la composición de las caseínas y con su carga eléctrica. Sin embargo su explicación es demasiado compleja como para tratarla aquí (si realmente estás interesado puedes consultar las fuentes que se recogen al final de este artículo).
Te animo a que hagas la prueba en casa. O a que se lo enseñes a tus hijos o alumnos ¡la ciencia es divertida!
Bebidas comerciales de leche y zumo

Sin embargo, si la cantidad de pectina que añadimos es excesiva, la pectina actuará como espesante: el calcio de la leche formará uniones con la pectina y aumentará notablemente la viscosidad, dando como resultado una textura no deseable. En definitiva, debemos añadir la cantidad justa de pectina. (Por cierto, este experimento también lo puedes hacer en casa. Puedes encontrar pectina en algunas farmacias y tiendas especializadas).
Siento que en esta ocasión las explicaciones sean un poco vagas, pero unas respuestas más certeras serían muy complejas y extensas (tanto la micela de caseína como la pectina son estructuras muy complejas y las reacciones en las que intervienen también lo son). (De hecho, a día de hoy ni siquiera se conoce con absoluta certeza la estructura de las micelas de caseína). Espero al menos haber saciado tu curiosidad sobre este tema.
Por otra parte, ¿no estás deseando que llegue el verano para probar esa bebida de nombre tan poético?
Fuentes
Este post está en la portada de Menéame. Muchas gracias por vuestro interés.





Sigo las entradas de tu Blog hace tiempo. Como siempre sublime en todos sus aspectos.
Si me permites una comparativa para "bien" , serias el heisenberg de Breaking Bad.
Un fuerte abrazo y sigue así.